缺氧誘導因子
| 缺氧誘導因子-1,α亞基 (hypoxia-inducible factor 1, alpha subunit) | |
|---|---|
| 識別 | |
| 符號 | HIF1A |
| Entrez | 3091 |
| HUGO | 4910 |
| OMIM | 603348 |
| RefSeq | NM_001530 |
| UniProt | Q16665 |
| 其他資料 | |
| 基因座 | 14 q21-q24 |
| 芳香烴受體核轉 (aryl hydrocarbon receptor nuclear translocator) | |
|---|---|
| 識別 | |
| 符號 | ARNT |
| 替換符號 | HIF1B, bHLHe2 |
| Entrez | 405 |
| HUGO | 700 |
| OMIM | 126110 |
| RefSeq | NM_001668 |
| UniProt | P27540 |
| 其他資料 | |
| 基因座 | 1 q21 |
| 內皮PAS域蛋白-1 (endothelial PAS domain protein 1) | |
|---|---|
| 識別 | |
| 符號 | EPAS1 |
| 替換符號 | HIF2A, MOP2, PASD2, HLF |
| Entrez | 2034 |
| HUGO | 3374 |
| OMIM | 603349 |
| RefSeq | NM_001430 |
| UniProt | Q99814 |
| 其他資料 | |
| 基因座 | 2 p21-p16 |
| 芳香烴受體核轉-2 (aryl-hydrocarbon receptor nuclear translocator 2) | |
|---|---|
| 識別 | |
| 符號 | ARNT2 |
| 替換符號 | HIF2B, KIAA0307, bHLHe1 |
| Entrez | 9915 |
| HUGO | 16876 |
| OMIM | 606036 |
| RefSeq | NM_014862 |
| UniProt | Q9HBZ2 |
| 其他資料 | |
| 基因座 | 1 q24 |
| 缺氧誘導因子-3,α亞基(hypoxia-inducible factor 3, alpha subunit) | |
|---|---|
| 識別 | |
| 符號 | HIF3A |
| Entrez | 64344 |
| HUGO | 15825 |
| OMIM | 609976 |
| RefSeq | NM_152794 |
| UniProt | Q9Y2N7 |
| 其他資料 | |
| 基因座 | 19 q13 |
缺氧誘導因子(Hypoxia-inducible factors,HIFs)是一種在細胞環境中的轉錄因子,因氧含量而產生不同反應的,主要是在氧氣減少或缺氧[1] 的情況下活化。
結構
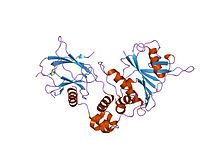
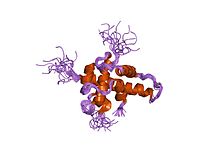
[編輯]大部分需要氧氣呼吸的物種,都擁有保守序列HIF-1。其轉錄都有嚴格的調控機制。HIF-1是由一個α亞基和一個β亞基組成的異源蛋白二聚體,而β亞基是一種芳香烴受體核轉位子(ARNT) [2][3]。 HIF-1屬於鹼性螺旋-環-螺旋(bHLH)家族中的PER-ARNT-SIM(PAS)亞家族。 α亞基和β亞基的結構類似,且都包含下列結構域[4][5][6]:
- N-末端 - 一個bHLH結構域,能和DNA結合。
- 中間區域 - Per-ARNT-Sim (PAS)結構域,有利於形成異源蛋白二聚體。
- C-末端 - 一個能與轉錄輔調節因子結合的蛋白質,促使轉錄共調節。
| ||||||||||||||||||||
| ||||||||||||||||||||||||||
成員
[編輯]下列為人類的 HIF 家族:
| 成員 | 基因 | 蛋白 |
|---|---|---|
| HIF-1α | HIF1A | 缺氧誘導因子-1,α亞基 |
| HIF-1β | HIF-1β | 芳香烴受體核轉 |
| HIF-2α | EPAS1 | 內皮PAS域蛋白-1 |
| HIF-2β | ARNT2 | 芳基烴受體核轉-2 |
| HIF-3α | HIF3A | 缺氧誘導因子-3,α亞基 |
| HIF-3β | ARNTL | 芳基烴受體核轉-3 |
作用
[編輯]在細胞中,HIF信號級聯反應會受到缺氧狀態的影響。在缺氧狀態下,通常會讓細胞持續的細胞分化。然而,缺氧狀態促進了血管新生,對於胚胎中的血管系統與癌症腫瘤來說非常重要。 傷口處的缺氧狀態,也促進了角質細胞的移動與上皮組織的修護[9]。
在普遍情況下,HIF是發育的重要關鍵。在哺乳動物中,若缺少了HIF-1的基因,將導致胎兒死亡。HIF-1已經被證實,對於軟骨細胞的存亡有重大的影響,他能使軟骨細胞適應在骨骼間生長板的缺氧環境。缺氧誘導因子在人類的代謝調節[10]中,屬於一個核心角色。
機制
[編輯]HIF中α亞基上的脯氨酸殘會透過HIF脯氨醯羥化酶羥基化,而使其能被 VHL E3泛素連接酶辨識並泛素化,之後透過蛋白酶體[11]使其被快速降解。這只會發生在含氧量正常的條件。但在缺氧條件下,HIF脯氨醯羥化酶會被抑制,因為它利用氧作為輔助基質[12]。
在琥珀酸去氫酶複合物中,電子轉移的抑制是因為SDHB或SDHD基因的突變,其會導致琥珀的積聚,進而抑制HIF脯氨醯羥化酶的活性,穩定HIF-1,α,這被稱為偽組織缺氧。
HIF-1,當持續在缺氧條件下,正向調節多種基因以能再低含氧量的情況下生存。 HIF-1能調節的酵素包括糖解作用酶,使其能以不耗氧的方式合成三磷酸腺苷;還有血管內皮生長因子(VEGF),能促進血管新生。HIF-1的觸發,是藉由HIF-反應元件(HREs)結合到了啟動子上的NCGTG序列。
已有實驗證明,肌A激酶錨定蛋白(mAKAP)組成的E3泛素連接酶能作用於HIF-1,影響其穩定性與定位,使其移動至細胞核中。 當 mAKAP 耗盡或因其他因素干擾 mAKAP 定位在細胞核(心肌細胞)周圍區域時,會影響了HIF的穩定性,與其他和缺氧相關基因的轉錄活性。因此,將對氧氣敏感的信號物件「區域化」,可能影響缺氧時反應的進行。[13]
在過去,與缺氧環境下HIF的調控機制資訊相較而言,含氧量正常時透過NF-κB介入的HIF調控機制和功能訊,尚處於不明確的狀況。同樣的,HIF-1α亞基的穩定性,在非缺氧環境下,其運作機制也是未知的。但近期指出,NF-κB(NF-κB)是HIF-1α在正常含氧量下的直接調節因子。以小干擾RNA作用在NF-κB上發現到,其會影響HIF-1α mRNA 的表現程度,因此證實了NF-κB能HIF-1α的表現。最後,當進行腫瘤壞死因子-α(TNAα)治療時,NF-κB被大量誘導表現,HIF-1α表現程度也受到影響[14]。HIF-1和HIF-2具有不同的生理作用。HIF-2用於調節成人體內的紅血球生成素。[15]
治療相關
[編輯]貧血
[編輯]最近,多種作用為選擇性的HIF脯氨醯羥化酶的抑制劑已經被開發了。[16] 其中最引人注目的包括FibroGen公司的化合物FG-2216和FG-4592[17][18],是兩個以口服方式治療[貧血]的藥物。[19]藉由抑制HIF脯氨醯羥化酶,使HIF-2α在腎的穩定性增加,這導致紅血球生成素的生產的[20]。這兩種藥物對II期臨床試驗已經成功了,但這些都在2007年5月暫停了,因為有試驗參發生暴發性肝炎死亡。不過,目前還不清楚肝炎死亡是否是由FG-2216所引起的。在2008年年初,因美國FDA的審查和批准,解除臨床試驗的暫停。 [21]
炎症和癌症
[編輯]在其它情況中,並接續上面的治療主題。最近的研究表明,在常氧狀態下誘導HIF表現,可能造成含有慢性炎性成分的疾病。且已經表明,慢性炎症是自我延續的,並且是因為微環境的異常,而導致轉錄因子被異常活化的結果。發生在細胞中,生長因子、趨化因子、細胞因子和活性氧平衡的改變,反過提供生長的需要,造成癌症發生與轉移。 最近發表的研究結果包含了許多病症,其中有NF-κB和HIF-1的失調,也有類風濕關節炎和癌症。因此,了解NF-κB和HIF兩著之間的關係,將大大提高藥物開發的發展。[14]
HIF的活性涉及到了血管新生,也造成腫瘤的生長,所以HIF的抑制劑,如異硫氰酸苯乙酯(Phenethyl isothiocyanate)和吖啶黃正在接受抗癌作用的測試。[22][23][24][25]
神經內科
[編輯]研究指出,在老鼠身上使用HIF脯氨醯羥化酶抑制劑,增強海馬體記憶,也增加了紅血球生成素的表現。[26]
另請參閱
[編輯]參考文獻
[編輯]- ^ Smith TG, Robbins PA, Ratcliffe PJ. The human side of hypoxia-inducible factor. Br. J. Haematol. May 2008, 141 (3): 325–34. PMC 2408651
 . PMID 18410568. doi:10.1111/j.1365-2141.2008.07029.x.
. PMID 18410568. doi:10.1111/j.1365-2141.2008.07029.x.
- ^ Wang GL, Jiang BH, Rue EA, Semenza GL. Hypoxia-inducible factor 1 is a basic helix-loop-helix-PAS heterodimer regulated by cellular O2 tension. Proc. Natl. Acad. Sci. U.S.A. June 1995, 92 (12): 5510–4. PMC 41725
 . PMID 7539918. doi:10.1073/pnas.92.12.5510.
. PMID 7539918. doi:10.1073/pnas.92.12.5510.
- ^ Jiang BH, Rue E, Wang GL, Roe R, Semenza GL. Dimerization, DNA binding, and transactivation properties of hypoxia-inducible factor 1. J. Biol. Chem. July 1996, 271 (30): 17771–8. PMID 8663540. doi:10.1074/jbc.271.30.17771.
- ^ Zhulin IB, Taylor BL, Dixon R. PAS domain S-boxes in Archaea, Bacteria and sensors for oxygen and redox. Trends Biochem. Sci. September 1997, 22 (9): 331–3. PMID 9301332. doi:10.1016/S0968-0004(97)01110-9.
- ^ Ponting CP, Aravind L. PAS: a multifunctional domain family comes to light. Curr. Biol. November 1997, 7 (11): R674–7. PMID 9382818. doi:10.1016/S0960-9822(06)00352-6.
- ^ Yang J, Zhang L, Erbel PJ, Gardner KH, Ding K, Garcia JA, Bruick RK. Functions of the Per/ARNT/Sim domains of the hypoxia-inducible factor. J. Biol. Chem. October 2005, 280 (43): 36047–54. PMID 16129688. doi:10.1074/jbc.M501755200.
- ^ Min JH, Yang H, Ivan M, Gertler F, Kaelin WG, Pavletich NP. Structure of an HIF-1alpha -pVHL complex: hydroxyproline recognition in signaling. Science. June 2002, 296 (5574): 1886–9. PMID 12004076. doi:10.1126/science.1073440.
- ^ Freedman SJ, Sun ZY, Poy F; et al. Structural basis for recruitment of CBP/p300 by hypoxia-inducible factor-1 alpha. Proc. Natl. Acad. Sci. U.S.A. April 2002, 99 (8): 5367–72. PMC 122775
 . PMID 11959990. doi:10.1073/pnas.082117899.
. PMID 11959990. doi:10.1073/pnas.082117899.
- ^ Benizri E, Ginouvès A, Berra E. The magic of the hypoxia-signaling cascade. Cell. Mol. Life Sci. April 2008, 65 (7-8): 1133–49. PMID 18202826. doi:10.1007/s00018-008-7472-0.
- ^ Formenti F, Constantin-Teodosiu D, Emmanuel Y, Cheeseman J, Dorrington KL, Edwards LM, Humphreys SM, Lappin TR, McMullin MF, McNamara CJ, Mills W, Murphy JA, O'Connor DF, Percy MJ, Ratcliffe PJ, Smith TG, Treacy M, Frayn KN, Greenhaff PL, Karpe F, Clarke K, Robbins PA. Regulation of human metabolism by hypoxia-inducible factor. Proc. Natl. Acad. Sci. U.S.A. July 2010, 107 (28): 12722–7. PMC 2906567
 . PMID 20616028. doi:10.1073/pnas.1002339107.
. PMID 20616028. doi:10.1073/pnas.1002339107.
- ^ Maxwell PH, Wiesener MS, Chang GW, Clifford SC, Vaux EC, Cockman ME, Wykoff CC, Pugh CW, Maher ER, Ratcliffe PJ. The tumour suppressor protein VHL targets hypoxia-inducible factors for oxygen-dependent proteolysis. Nature. May 1999, 399 (6733): 271–5. PMID 10353251. doi:10.1038/20459.
- ^ Semenza GL. Hydroxylation of HIF-1: oxygen sensing at the molecular level. Physiology (Bethesda). August 2004, 19 (4): 176–82. PMID 15304631. doi:10.1152/physiol.00001.2004.
- ^ Wong W, Goehring AS, Kapiloff MS, Langeberg LK, Scott JD. mAKAP compartmentalizes oxygen-dependent control of HIF-1alpha. Sci Signal. 2008, 1 (51): ra18. PMC 2828263
 . PMID 19109240. doi:10.1126/scisignal.2000026.
. PMID 19109240. doi:10.1126/scisignal.2000026.
- ^ 14.0 14.1 van Uden P, Kenneth NS, Rocha S. Regulation of hypoxia-inducible factor-1alpha by NF-kappaB. Biochem J. 2008, 412 (3): 477–484 [2022-03-25]. PMC 2474706
 . PMID 18393939. doi:10.1042/BJ20080476. (原始內容存檔於2019-09-02).
. PMID 18393939. doi:10.1042/BJ20080476. (原始內容存檔於2019-09-02).
- ^ Haase VH. Hypoxic regulation of erythropoiesis and iron metabolism. Am. J. Physiol. Renal Physiol. July 2010, 299 (1): F1–13. PMC 2904169
 . PMID 20444740. doi:10.1152/ajprenal.00174.2010.
. PMID 20444740. doi:10.1152/ajprenal.00174.2010.
- ^ Bruegge K, Jelkmann W, Metzen E. Hydroxylation of hypoxia-inducible transcription factors and chemical compounds targeting the HIF-alpha hydroxylases. Curr. Med. Chem. 2007, 14 (17): 1853–62. PMID 17627521. doi:10.2174/092986707781058850.
- ^ Dead URL FG-2216: Anemia 網際網路檔案館的存檔,存檔日期2008-09-28.
- ^ 存档副本. [2009-05-19]. (原始內容存檔於2011-07-10).
- ^ Cases A. The latest advances in kidney diseases and related disorders. Drug news & perspectives. December 2007, 20 (10): 647–54. ISSN 0214-0934. PMID 18301799.
- ^ Hsieh MM, Linde NS, Wynter A, Metzger M, Wong C, Langsetmo I, Lin A, Smith R, Rodgers GP, Donahue RE, Klaus SJ, Tisdale JF. HIF prolyl hydroxylase inhibition results in endogenous erythropoietin induction, erythrocytosis, and modest fetal hemoglobin expression in rhesus macaques. Blood. September 2007, 110 (6): 2140–7. PMC 1976368
 . PMID 17557894. doi:10.1182/blood-2007-02-073254.
. PMID 17557894. doi:10.1182/blood-2007-02-073254.
- ^ The FDA Accepts the Complete Response for Clinical Holds of FG-2216/FG-4592 for the Treatment of Anemia (PDF). [2014-06-22]. (原始內容 (PDF)存檔於2015-09-23).
- ^ KangAe Lee, Huafeng Zhang, David Z. Qian, Sergio Rey, Jun O. Liu, Gregg L. Semenza. Acriflavine inhibits HIF-1 dimerization, tumor growth, and vascularization. Proceedings of the National Academy of Sciences. 2009-10-20, 106 (42): 17910–17915 [2018-04-02]. doi:10.1073/pnas.0909353106.
- ^ Syed Alwi SS, Cavell BE, Telang U, Morris ME, Parry BM, Packham G. In vivo modulation of 4E binding protein 1 (4E-BP1) phosphorylation by watercress: a pilot study. Br. J. Nutr. November 2010, 104 (9): 1288–96. PMID 20546646. doi:10.1017/S0007114510002217.
- ^ Semenza GL. Evaluation of HIF-1 inhibitors as anticancer agents. Drug Discov. Today. October 2007, 12 (19-20): 853–9. PMID 17933687. doi:10.1016/j.drudis.2007.08.006.
- ^ Melillo G. Inhibiting hypoxia-inducible factor 1 for cancer therapy. Mol. Cancer Res. September 2006, 4 (9): 601–5. PMID 16940159. doi:10.1158/1541-7786.MCR-06-0235.
- ^ Bartosz Adamcio, Swetlana Sperling, Nora Hagemeyer, Gail Walkinshaw, Hannelore Ehrenreich. Hypoxia inducible factor stabilization leads to lasting improvement of hippocampal memory in healthy mice. Behavioural Brain Research. 2010-03-17, 208 (1): 80–84 [2019-02-12]. ISSN 1872-7549. PMID 19900484. doi:10.1016/j.bbr.2009.11.010. (原始內容存檔於2019-07-22).