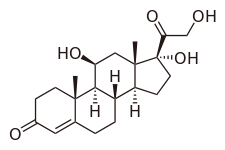
皮质醇
 | |
 | |
| 临床资料 | |
|---|---|
| 怀孕分级 |
|
| 给药途径 | 口服、静脉注射 |
| ATC码 | |
| 识别信息 | |
| |
| CAS号 | 50-23-7 |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.000.019 |
| 化学信息 | |
| 化学式 | C21H30O5 |
| 摩尔质量 | 362.465 |
| 3D模型(JSmol) | |
| |
| |
皮质醇(英语:cortisol)[1]又称氢化可的松(hydrocortisone),前者指人或动物肾上腺分泌的糖皮质激素,后者多作为药物使用时的名称(多为人工合成)[2]。皮质醇属于一种肾上腺皮质激素,具有促进肝糖原分解、糖异生,调节微循环和维持血压的作用,且有抗炎活性;由于在应付压力中扮演重要角色,故又称为“压力荷尔蒙”,会提高血压、血糖水平和产生免疫抑制作用。
在药理学的使用上,氢化可的松除了可补充皮质醇不足外,也可治疗过敏症和发炎。最初用作治疗类风湿性关节炎时,皮质醇被称作 Compound E(化合物E)。
生理反应
[编辑]血液中皮质醇含量在日中会变化,早上的水平最高,下降至午夜时最低。刚出生婴孩的皮质醇日中含量变化并非跟随上述规律;相关规律成形于两周至九个月大。[3]有关昼夜节律的讯息,相信由视网膜传送至下丘脑的视交叉上核)。
研究发现,特定的皮质醇水平变化与失常的促肾上腺皮质素水平、忧郁症、压力有关,也与血糖过低、疾病、发热、创伤、恐惧、痛楚和极端温度等会引起因压力而来之生理反应的事件有关。
作用
[编辑]正常含量的皮质醇(如其他糖皮质激素)有助身体在压力下回复体内平衡。长期压力会导致长时间分泌皮质醇。
- 胰岛素
皮质醇提高糖原分解和脂类、蛋白质的分解,促进制造肝外氨基酸和酮类,变相中和胰岛素作用。这会间接增加血液中的葡萄糖含量,肝脏也会增加分解糖原。[4]长期分泌皮质醇会导致多糖症。
- 氨基酸
皮质醇通过抑制胶原质形成、减低肌肉吸收氨基酸和抑制蛋白质合成,提升血清中的氨基酸含量。[5]
皮质醇会刺激胃酸分泌[6],从而增加腹泻时钾和酸的流失。
- 钠代谢
皮质醇有助哺乳类动物抑制钠从肠流失。[7]但钠的流失不影响皮质醇分泌[8]。
- 钾代谢
皮质醇会导致钾从细胞流失,主要通过补回同等数目的钠来实现。[9]这较不会影响身体pH值,因为正常来说每3个钾离子流失只会有2个钠离子补回。
- 水代谢
- 铜代谢
皮质醇可增加免疫作用中铜的含量,从而刺激含铜的酵素[10],包括超氧化物歧化酶(superoxide dismutase)[11],该种酶用作抵抗细菌。
- 免疫系统
- 骨骼代谢
- 记忆
皮质醇与肾上腺素对产生短期情绪记忆有重要作用,有关机制被认为可能帮助记忆日后要逃避的事物。不过,长时期过多皮质醇会损害海马体,影响学习能力。
- 其他作用
失调
[编辑]皮质醇与ACTH的关系如下:
| 血液皮质醇含量 | 血液ACTH含量 | |
|---|---|---|
| 主皮质醇过高(库兴氏症候群) | ↑ | ↓ |
| 副皮质醇过高(脑垂体,库兴氏症候群) | ↑ | ↑ |
| 主皮质醇过低(爱迪生氏病) | ↓ | ↑ |
| 副皮质醇过低(脑垂体) | ↓ | ↓ |
药理学
[编辑]
氢羟肾上腺皮质素是皮质醇的化学物形式,可用作口服或静脉注射,有免疫抑制作用,以注射方式治疗过敏反应和血管性水肿等过敏症,也会用作治疗发炎。
补充剂可体纤的制造商声称通过抑遏皮质醇可降低体重,制造商在2007年因虚假广告被美国联邦贸易委员会罚款1200万美元,该制造商不再声称可体纤可抑制皮质醇。
合成
[编辑]皮质醇合成于肾上腺皮质。
参见
[编辑]参考文献
[编辑]- ^ 存档副本. [2023-12-18]. (原始内容存档于2023-12-18).
- ^ 存档副本. [2023-12-18]. (原始内容存档于2023-12-18).
- ^ de Weerth C, Zijl R, Buitelaar J. Development of cortisol circadian rhythm in infancy. Early Hum Dev. 2003, 73 (1-2): 39–52. PMID 12932892.
- ^ Freeman, Scott (2002). Biological Science. Prentice Hall; 2nd Pkg edition(December 30, 2004). ISBN 0-13-218746-9.
- ^ Manchester, K.L.,“Sites of Hormonal Regulation of Protein Metabolism. p. 229”, Mammalian Protein [Munro, H.N., Ed.]. Academic Press, New York. On p273.
- ^ Soffer, L.J.; Dorfman, R.I.; Gabrilove, J.L,. “The Human Adrenal Gland”. Febiger, Phil.
- ^ 7.0 7.1 Sandle, G.I.; Keir, M.G.; Record, CO.(1981)“The Effect of Hydrocortisone on the Transport of Water, Sodium, and Glucose in the Jejunum”. Scandinavian Journal of Gastroenterol. 16: 667,.
- ^ Mason, P.A.; Fraser, R.; Morton, J.J.(1977)“The Effect of Sodium Deprivation and of Angiotensin II Infusion on the Peripheral Plasma Concentration of 18 Hydroxycorticosterone, Aldosterone, and Other Corticosteoids in Man”. Steroid Biochemistry 8: 799,
- ^ Knight, R.P., Jr.; Kornfield, D.S.; Glaser, G.H. & Bondy, P.K.(1955)“Effects of Intravenous Hydrocortisone on Electrolytes in Serum and Urine in Man”. Journal of Clinical Endocrinology 15: 176-181,.
- ^ Weber, C.E(1984)。“Copper Response to Rheumatoid Arthritis”. Medical Hypotheses 15: 333-348, on p337,.
- ^ Flohe, L.; Beckman, R.; Giertz, H.; Loschen, G. “Oxygen Centered Free Radicals as Mediators of Inflammation. p. 405”, Oxidative Stress(Sies H, ed)Academic Press, New York.
- ^ Palacios R., Sugawara I. Hydrocortisone abrogates proliferation of T cells in autologous mixed lymphocyte reaction by rendering the interleukin-2 Producer T cells unresponsive to interleukin-1 and unable to synthesize the T-cell growth factor. Scand J Immunol. 1982, 15 (1): 25–31. PMID 6461917. doi:10.1111/j.1365-3083.1982.tb00618.x.
