親核共軛加成

親核共軛加成是一種有關共軛不飽和有機化合物的加成反應。一般的親核加成(或稱1,2-親核加成)反應加成在羰基化合物上。簡單的烯烴化合物由於缺乏極性,不會有1,2-親核加成的反應性,除非有特殊的取代基活化烯烴。α,β-不飽和羰基化合物(像環己烯酮)可以由共振結構推斷β位是親電子位點,可以與親核試劑反應。結構中的負電荷可以醇鹽陰離子的形式存在。這樣的親核加成反應稱做親核共軛加成或1,4-親核加成。而最重要的活性烯烴是上述提到的共軛羰基和丙烯腈。
反應機制
[編輯]共軛加成是符合插烯原則(化合物的鍵結為單雙單雙)的親核加成反應。親核試劑與α,β-不飽和羰基化合物的β位置反應。親核試劑所帶負電荷因離域化,在醇鹽陰離子和有α碳原子的碳負離子二組組態之間共振。質子化反應通過酮-烯醇互變異構產生飽和羰基化合物。相鄰兩個官能基的氫則由另一個親電試劑取代。
反應
[編輯]- 共軛羰基化合物與二級胺反應以形成1,4-酮胺。
- 共軛羰基化合物與氰化氫反應產生1,4-酮醯基。在Nagata反應中,氰化物是由二乙基氰化鋁提供。
- 吉爾曼試劑是對1,4-共軛羰基有效的親核試劑。
- 麥可加成反應是烯醇的共軛加成,產物是羰基的共軛化合物。
- 施托克烯胺反應是烯胺的共軛加成,產物到羰基的共軛化合物。
應用
[編輯]在有機金屬試劑的存在下,親核共軛加成是有效的形成碳-碳鍵的反應。例如甲基乙烯基酮和有機鋅碘化物反應。
![(4R',5R')-5-(5-Ethyl-2,2-dimethyl-[1,3]-dioxolan-4-yl) -pentan-2-one](http://upload.wikimedia.org/wikipedia/commons/7/7b/Conjugateadditionexample.png)
以下是一個不對稱合成的共軛加成例子:環己烯酮和苯硼酸反應,加上銠乙醯丙酮催化劑及手性配體的BINAP,最後合成(R)-3-苯基-環己酮。

另一個不對稱合成的例子:α,β-不飽和羰基化合物首先和掌性咪唑酮催化劑及掌性輔助劑通過胺羰縮合反應反應生成亞胺,然後亞胺以鏡像選擇性地與親核試劑呋喃反應生成親核性的烯胺。接著烯胺與親電試劑氯代苯醌發生級聯反應。最後脫去咪唑烷酮催化劑,得到產物。總的來看,該α,β-不飽和羰基化合物經過串聯反應後被親核試劑和親電試劑以順反產物比8:1和97%對映體過剩率(ee)有效地官能化。
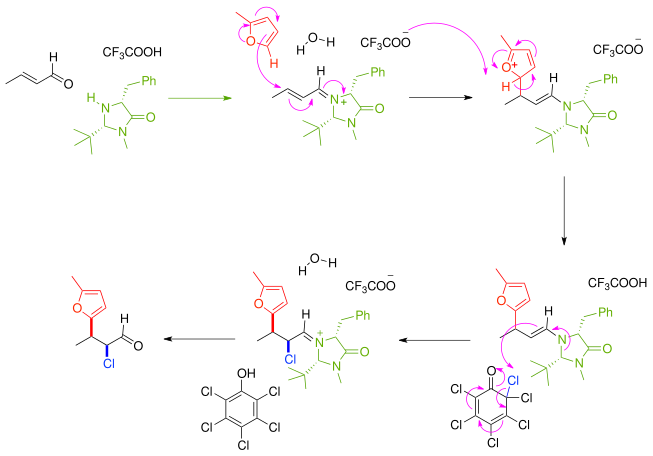
這一合成原理也適用於多組分反應鏡像選擇性的硫醇級聯親核共軛加成反應,例如苯甲基硫醇和親電性的偶氮二甲酸二乙酯反應。

毒理學
[編輯]可溶性的Michael受體會利用共軛加成,使DNA烷基化引起突變,因此具有細胞毒性及致癌性。然而,穀胱甘肽及富馬酸二甲酯也能夠與Michael受體反應。
參見
[編輯]參考文獻
[編輯]- Conjugate addition (頁面存檔備份,存於網際網路檔案館)
- ^ Andréa L. de Sousa & Inês S. Resck. Asymmetric Synthesis of exo-Isobrevicomin and exo-Brevicomin via Conjugated Addition of Primary Alkyl Iodides to α,β-Unsaturated Ketones. J. Braz. Chem. Soc. 2002, 13 (2): 233. doi:10.1590/S0103-50532002000200015.
- ^ Tamio Hayashi, Makoto Takahashi, Yoshiaki Takaya, and Masamichi Ogasawara (2004). "(R)-3-phenyl-cyclohexanone". Org. Synth.; Coll. Vol. 10: 609.
- ^ Yong Huang; Abbas M. Walji; Catharine H. Larsen; David W. C. MacMillan. Enantioselective Organo-Cascade Catalysis. J. Am. Chem. Soc. Nov 2005, 127 (43): 15051–15053. ISSN 0002-7863. PMID 16248643. doi:10.1021/ja055545d.
- ^ Mauro Marigo; Tobias Schulte; Johan Franzén & Karl Anker Jorgensen. Asymmetric Multicomponent Domino Reactions and Highly Enantioselective Conjugated Addition of Thiols to α,β-Unsaturated Aldehydes. J. Am. Chem. Soc. Nov 2005, 127 (45): 15710–15711. ISSN 0002-7863. PMID 16277506. doi:10.1021/ja055291w.
