甲硫氨酸
| 甲硫氨酸(蛋胺酸) Methionine | |
|---|---|

| |

| |

| |
| IUPAC名 Methionine 2-氨基-4-甲硫基丁酸 | |
| 别名 | 甲硫胺酸 2-amino-4-(methylthio)butanoic acid |
| 识别 | |
| 缩写 | Met, M |
| CAS号 | 59-51-8 63-68-3((L-isomer)) 348-67-4((D-isomer)) |
| PubChem | 876 |
| ChemSpider | 853, 5907 (L-isomer) |
| SMILES |
|
| InChI |
|
| ChEBI | 16811 |
| KEGG | D04983 |
| 性质 | |
| 化学式 | C5H11NO2S |
| 摩尔质量 | 149.21 g·mol−1 |
| 外观 | 白色晶状粉末 |
| 密度 | 1.340 g/cm3 |
| 熔点 | 281 °C(554 K)(分解) |
| 溶解性(水) | 可溶 |
| pKa | 2.28 (羧基), 9.21 (氨基)[1] |
| 药理学 | |
| ATC代码 | V03AB26(V03),QA05, QG04 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
甲硫氨酸(英语:Methionine, /mɪˈθaɪəniːn/[2]),又称蛋胺酸,可简写为“Met”或“M”[3],在所有后生动物中它是一种必需氨基酸。与半胱氨酸一起,甲硫氨酸是两个含硫蛋白原氨基酸之一。对人而言是唯一的含硫必需氨基酸,由mRNA上担任起始密码子的AUG密码子编码。甲硫氨酸最早由美国生物化学家约翰·霍华德·穆勒于1921年分离提纯[4]。
甲硫氨酸与生物体内各种含硫化合物的代谢密切相关、是体内活性甲基和硫的主要来源[5]。甲硫氨酸在血管新生过程中发挥重要作用,此外,甲硫氨酸也是一种解毒剂,能通过提供巯基够缓解铜中毒等重金属中毒[6][7]。
化学结构
[编辑]甲硫氨酸是一种α-氨基酸。换言之,甲硫氨酸的氨基与羧基都与α碳相连,其侧链是一个硫醚基团,因此分子极性较低,可归类为非极性氨基酸。与另一种含硫氨基酸半胱氨酸不同,甲硫氨酸亲核性不强,不过仍然可以与一部分亲电分子反应[8]。
甲硫氨酸有L型及D型两种,天然状态下的甲硫氨酸基本都是L型[5]。
生物化学
[编辑]甲硫氨酸由mRNA上的AUG密码子编码,这个密码子位于开放读框第一位时,也是起始密码子。甲硫氨酸通常位于蛋白质内部,一般不参与酶活性中心的共价催化[8]。
在人体内,甲硫氨酸对血管新生相当重要。对于重金属中毒患者,甲硫氨酸能够通过提供巯基缓解中毒症状[6]。一些研究表明限制甲硫氨酸摄入能够提高动物寿命,但这种现象是否具有普适性依然存在争议[5]。另外,甲硫氨酸可能会经由提供甲基基团影响DNA甲基化,进而对肿瘤生长产生影响[9][10]。
合成与代谢
[编辑]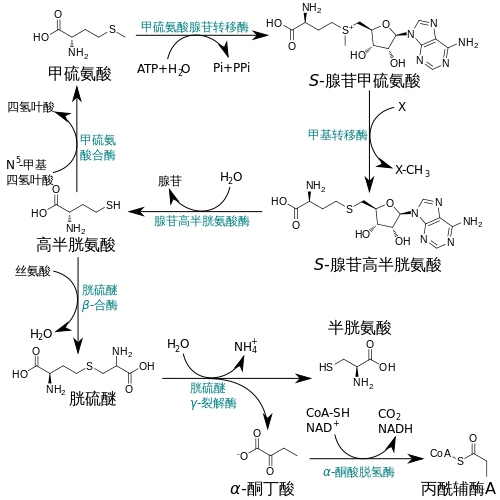
大部分细菌、真菌,以及植物都具有以天冬氨酸为底物合成甲硫氨酸的能力[11],但包括人类在内的动物无法自主合成甲硫氨酸,因此必须摄入甲硫氨酸才能维持生存。因此,对人类以及牲畜来说,甲硫氨酸是一种必需氨基酸[5]。因动物饲料中通常会缺乏甲硫氨酸,一种弥补措施是添加甲硫氨酸进行补强[5][12]。
代谢方面,生物体内的甲硫氨酸一般先由甲硫氨酸腺苷转移酶转化为甲基供体S-腺苷甲硫氨酸(SAM)。S-腺苷甲硫氨酸失去甲基之后,会转化为S-腺苷-L-高半胱氨酸(SAH)。S-腺苷-L-高半胱氨酸可经由水解作用生成高半胱氨酸,再经由转硫通路转化为半胱氨酸,或借助四氢叶酸提供的甲基重新转化为甲硫氨酸[13]。
代谢性疾病
[编辑]以下代谢性疾病会影响蛋氨酸的降解。
- 结合性丙二酸及甲基丙二酸血症 (CMAMMA)
- 高胱胺酸尿症
- 甲基丙二酸血症
- 丙酸血症
工业合成
[编辑]工业上通常使用甲硫醇、丙烯醛和氰化氢合成甲硫氨酸[5][14]。工业合成的甲硫氨酸产品中同时含有D-甲硫氨酸与L-甲硫氨酸。为了满足制药等行业的需求,可以使用酶将同时含有D-甲硫氨酸与L-甲硫氨酸的产品转化为纯L-甲硫氨酸[5]。
参考文献
[编辑]- ^ Dawson, R.M.C.; et al. Data for Biochemical Research. Oxford: Clarendon Press. 1959.
- ^ Methionine. Oxford University Press. [2021-08-09]. (原始内容存档于2018-06-12).
- ^ Nomenclature and Symbolism for Amino Acids and Peptides. IUPAC-IUB Joint Commission on Biochemical Nomenclature. 1983 [5 March 2018]. (原始内容存档于9 October 2008).
- ^ Pappenheimer AM. A Biographical Memoir of John Howard Mueller (PDF). Washington D.C.: National Academy of Sciences. 1987 [2021-08-09]. (原始内容存档 (PDF)于2021-10-13).
- ^ 5.0 5.1 5.2 5.3 5.4 5.5 5.6 Willke, Thomas. Methionine production—a critical review. Applied Microbiology and Biotechnology. 2014, 98 (24): 9893–9914. ISSN 0175-7598. doi:10.1007/s00253-014-6156-y.
- ^ 6.0 6.1 Methionine. WebMD. [2021-08-09]. (原始内容存档于2017-09-12).
- ^ 张天民; 张瑞菊. 食品安全与健康. 2011: 161 [2021-08-09]. ISBN 978-7-5019-7890-8. (原始内容存档于2021-10-16).
- ^ 8.0 8.1 Methionine M (Met). University of Arizona. [2021-08-09]. (原始内容存档于2021-08-09).
- ^ Cavuoto P, Fenech MF. A review of methionine dependency and the role of methionine restriction in cancer growth control and life-span extension. Cancer Treatment Reviews. 2012, 38 (6): 726–36. PMID 22342103. doi:10.1016/j.ctrv.2012.01.004.
- ^ Cellarier E, Durando X, Vasson MP, Farges MC, Demiden A, Maurizis JC, Madelmont JC, Chollet P. Methionine dependency and cancer treatment. Cancer Treatment Reviews. 2003, 29 (6): 489–99. PMID 14585259. doi:10.1016/S0305-7372(03)00118-X.
- ^ Ferla, Matteo P.; Patrick, Wayne M. Bacterial methionine biosynthesis. Microbiology. 2014, 160 (8): 1571–1584. ISSN 1350-0872. doi:10.1099/mic.0.077826-0.
- ^ Rules and Regulations. Federal Register. March 14, 2011, 76 (49): 13501–13504 [2021-08-09]. (原始内容存档于2011-07-21).
- ^ Sanderson, Sydney M.; Gao, Xia; Dai, Ziwei; Locasale, Jason W. Methionine metabolism in health and cancer: a nexus of diet and precision medicine. Nature Reviews Cancer. 2019, 19 (11): 625–637. ISSN 1474-175X. doi:10.1038/s41568-019-0187-8.
- ^ Karlheinz Drauz, Ian Grayson, Axel Kleemann, Hans-Peter Krimmer, Wolfgang Leuchtenberger, Christoph Weckbecker, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, 2005, doi:10.1002/14356007.a02_057.pub2
参看
[编辑]外部链接
[编辑]- Rudra, M. N.; Chowdhury, L. M. Methionine Content of Cereals and Legumes. Nature. 30 September 1950, 166 (568): 568. Bibcode:1950Natur.166..568R. doi:10.1038/166568a0.

