阿扎胞苷
 | |
| 临床资料 | |
|---|---|
| 商品名 | Vidaza, Azadine, Onureg |
| 其他名称 | 5-Azacytidine (5-AZA), Azacytidine, Ladakamycin, 4-Amino-1-β-D-ribofuranosyl-s-triazin-2(1H)-one, U-18496, CC-486 |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a607068 |
| 核准状况 |
|
| 怀孕分级 | |
| 给药途径 | 皮下注射、静脉注射、口服 |
| ATC码 | |
| 法律规范状态 | |
| 法律规范 |
|
| 药物动力学数据 | |
| 药物代谢 | 主要经肾排出,部分可能经肝代谢 |
| 生物半衰期 | 4小时[3] |
| 识别信息 | |
| |
| CAS号 | 320-67-2 |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.005.711 |
| 化学信息 | |
| 化学式 | C8H12N4O5 |
| 摩尔质量 | 244.21 g·mol−1 |
| 3D模型(JSmol) | |
| |
| |
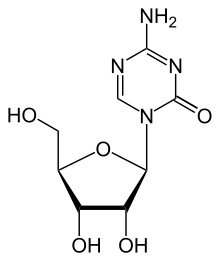
阿扎胞苷(INN:Azacitidine),有时也称为5-阿扎胞苷(5-Azacitidine),商品名维达莎或委丹扎(Vidaza),是一种胞苷(组成DNA与RNA的核苷之一)类似物,由捷克斯洛伐克学者弗朗蒂斯克·索姆(František Šorm)于20世纪60年代首先合成用于肿瘤化疗[4],目前主要用于治疗骨髓增生异常综合征[5]。阿扎胞苷目前也是一种在生物医学研究中常用的DNA甲基化抑制剂[6][7]。
作用机理
[编辑]阿扎胞苷是一种胞苷类似物。在低剂量时,阿扎胞苷能够通过与DNA甲基化酶DNMT蛋白家族形成共价键抑制其酶活性,使细胞的DNA甲基化水平降低[9][10]。因为阿扎胞苷的这一性质,在生物医学研究中,研究者常常将阿扎胞苷用作DNA甲基化抑制剂[7]。而在高剂量时,阿扎胞苷能直接插入细胞的DNA与RNA中,分别干扰DNA代谢和阻断RNA翻译的过程,从而抑制蛋白质的合成,由此产生细胞毒性,令细胞死亡[11][12]。
药代动力学
[编辑]经皮下注射后,阿扎胞苷能快速被吸收,生物利用度可达89%。在人体内阿扎胞苷的半衰期约为4小时。代谢方面,主要经肾脏排出[13]。
毒性
[编辑]阿扎胞苷可能造成贫血、嗜中性白血球低下,以及血小板减少症等药物不良反应[2]。此外,在存在严重肝功能障碍的病人中,阿扎胞苷可能产生肝毒性。与其他化疗药物同时使用时,可能造成程度不一的肾毒性[2]。此外,也有过量给予阿扎胞苷造成患者腹泻、恶心和呕吐的报告[13]。
临床应用
[编辑]目前阿扎胞苷主要用于治疗骨髓增生异常综合征。2004年,美国食品药品监督管理局(FDA)批准将阿扎胞苷用于骨髓增生异常综合征治疗中[10]。除此之外,阿扎胞苷偶尔也被用于急性骨髓性白血病的化学治疗中[14]。
此外,一些动物实验结果表明阿扎胞苷有抗病毒作用,但目前为止阿扎胞苷尚未被批准用于抗病毒治疗中[15][16]。
参见
[编辑]参考文献
[编辑]- ^ 1.0 1.1 Azacitidine (Vidaza) Use During Pregnancy. Drugs.com. 2020-05-05 [2020-08-12]. (原始内容存档于2020-12-05).
- ^ 2.0 2.1 2.2 Vidaza- azacitidine injection, powder, lyophilized, for solution. DailyMed. 2020-03-02 [2020-09-27]. (原始内容存档于2021-11-05). 引用错误:带有name属性“Vidaza FDA label”的
<ref>标签用不同内容定义了多次 - ^ Vallerand, April Hazard; Deglin, Judith Hopfer. Davis's drug guide for nurses.. Philadelphia: F.A. Davis Company. 2009: 204–206. ISBN 978-0-8036-1912-8.
- ^ Khan, Cyrus; Pathe, Neeta; Fazal, Salman; Lister, John; Rossetti, James M. Azacitidine in the management of patients with myelodysplastic syndromes. Therapeutic Advances in Hematology. 2012, 3 (6): 355–373. ISSN 2040-6207. doi:10.1177/2040620712464882.
- ^ Buckstein, Rena; Yee, Karen; Wells, Richard A. 5-Azacytidine in myelodysplastic syndromes: A clinical practice guideline. Cancer Treatment Reviews. 2011, 37 (2): 160–167. ISSN 0305-7372. doi:10.1016/j.ctrv.2010.05.006.
- ^ Christina M. Bender; etal. Inhibition of DNA Methylation by 5-Aza-2′-deoxycytidine Suppresses the Growth of Human Tumor Cell Lines. Cancer Research. 1998, 58 (1) [2021-03-28]. PMID 9426064.
- ^ 7.0 7.1 Jones, P. A.; Taylor, S. M.; Wilson, V. L. Inhibition of DNA Methylation by 5-Azacytidine: 202–211. 1983. doi:10.1007/978-3-642-81947-6_15.
- ^ Derissen, Ellen J.B.; Beijnen, Jos H.; Schellens, Jan H.M. Concise Drug Review: Azacitidine and Decitabine. The Oncologist. 2013, 18 (5): 619–624. ISSN 1083-7159. doi:10.1634/theoncologist.2012-0465.
- ^ Sprangers, Ben; Cosmai, Laura; Porta, Camillo. Conventional chemotherapy: 127–153.e11. 2020. doi:10.1016/B978-0-323-54945-5.00025-4.
- ^ 10.0 10.1 Raj, Kavita; Mufti, Ghulam J. Azacytidine (Vidaza) in the treatment of myelodysplastic syndromes. Therapeutics and Clinical Risk Management. 2006, 2 (4): 377–388. ISSN 1176-6336. doi:10.2147/tcrm.2006.2.4.377.
- ^ Zhu, Wei; Qian, Jiaqi. Clinical Trials: 525–568. 2015. doi:10.1016/B978-0-12-800206-3.00023-9.
- ^ Gerson, Stanton L.; Caimi, Paolo F.; William, Basem M.; Creger, Richard J. Pharmacology and Molecular Mechanisms of Antineoplastic Agents for Hematologic Malignancies: 849–912. 2018. doi:10.1016/B978-0-323-35762-3.00057-3.
- ^ 13.0 13.1 Azacitidine. Drugbank. [2021-03-28]. (原始内容存档于2021-05-17).
- ^ Estey EH. Epigenetics in clinical practice: the examples of azacitidine and decitabine in myelodysplasia and acute myeloid leukemia. Leukemia. September 2013, 27 (9): 1803–12. PMID 23757301. doi:10.1038/leu.2013.173.
- ^ Wang X, Zou P, Wu F, Lu L, Jiang S. Development of small-molecule viral inhibitors targeting various stages of the life cycle of emerging and re-emerging viruses. Frontiers of Medicine. December 2017, 11 (4): 449–461. PMC 7089273
 . PMID 29170916. doi:10.1007/s11684-017-0589-5.
. PMID 29170916. doi:10.1007/s11684-017-0589-5.
- ^ Ianevski A, Zusinaite E, Kuivanen S, Strand M, Lysvand H, Teppor M, et al. Novel activities of safe-in-human broad-spectrum antiviral agents. Antiviral Research. June 2018, 154: 174–182. PMC 7113852
 . PMID 29698664. doi:10.1016/j.antiviral.2018.04.016. hdl:10138/301108.
. PMID 29698664. doi:10.1016/j.antiviral.2018.04.016. hdl:10138/301108.
