箭毒蛙碱
此条目可参照英语维基百科相应条目来扩充。 |
| 箭毒蛙碱 | |
|---|---|
| |
| |

| |
| 识别 | |
| CAS号 | 23509-16-2 |
| PubChem | 6324647 |
| ChemSpider | 10310314 |
| SMILES |
|
| InChI |
|
| InChIKey | ISNYUQWBWALXEY-OMIQOYQYBY |
| IUPHAR配体 | 2619 |
| 性质 | |
| 化学式 | C31H42N2O6 |
| 摩尔质量 | 538.67 g·mol−1 |
| 密度 | 1.304 g/mL [1] |
| 危险性 | |
| 主要危害 | 剧毒 |
| 致死量或浓度: | |
LD50(中位剂量)
|
2 μg/kg (mouse, sub-cutaneous) |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
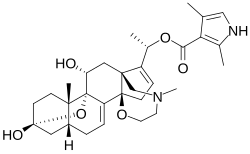
箭毒蛙碱(英语:Batrachotoxin,缩写:BTX)是一种极强的心脏和神经毒性甾体生物碱,存在于某些甲虫、鸟类和青蛙物种中。这个名字来自希腊词“βάτραχος”,意思即为“青蛙”。[2]与此结构相关的化合物通常统称为箭毒蛙碱,它是一种剧毒的生物碱,在某些青蛙中,这种生物碱主要存在于皮肤上,这种青蛙是美洲原住民用于制作毒镖的青蛙之一。箭毒蛙碱与神经细胞的钠离子通道结合,并使其不可逆转地打开,阻止它们关闭,导致瘫痪和死亡,目前没有任何已知的解毒剂。
历史
[编辑]Batrachotoxin是由Fritz Märki和Bernhard Witkop在美国马里兰州贝塞斯达国立卫生研究院的国立关节炎和代谢疾病研究所发现的。Märki和Witkop于1963年从双色叶状藻中分离出强毒性生物碱成分,并确定了其化学性质。[3]他们分离出四种主要的有毒甾体生物碱,包括箭毒蛙碱、异箭毒蛙碱、伪箭毒蛙碱和箭毒蛙碱A。[4]由于要处理如此强效的毒素很困难,而且可以收集到的数量很少,因此在全面的结构测定遇到了一些困难。然而,后来加入调查的Takashi Tokuyama将其中一种同源化合物箭毒蛙碱A转化为结晶衍生物,并用X射线衍射技术解析了其独特的甾体结构(1968年)。[5]比较箭毒蛙碱和箭毒蛙碱A衍生物的质谱和NMR光谱时,发现两者俱有相同的甾体结构,箭毒蛙碱是 带有单个额外吡咯部分的箭毒蛙碱A。
毒性
[编辑]根据啮齿动物的实验,箭毒蛙碱是已知毒性最强的生物碱之一:它在小鼠体内的静脉注射半致死剂量为2-3 µg/kg。[5]同时,它的衍生物batrachotoxinin A的毒性要低得多,半致死剂量为1000 µg/kg。[4]
毒素通过叶箭毒蛙属青蛙的背部和耳朵后面的腺体的无色或乳状分泌物释放。当青蛙激动、感觉受到威胁或感到疼痛时,毒素会通过几条管道反射性地释放出来。
神经毒性
[编辑]箭毒蛙碱是一种神经毒素,它会影响神经系统。由于可兴奋细胞膜的钠离子渗透性增加,神经功能取决于神经和肌肉纤维的去极化。脂溶性毒素如箭毒蛙碱直接作用于参与动作电位产生的钠离子通道[6],并改变它们的离子选择性和电压敏感性。箭毒蛙碱不可逆地与钠离子通道结合,导致通道中的构象发生变化,从而迫使钠离子通道保持开放。箭毒蛙碱不仅使电压门控钠离子通道保持打开状态,而且还降低了单通道电导。换句话说,毒素与钠离子通道结合,并以“全有或全无”的方式保持膜对钠离子的通透。[7]
箭毒蛙碱对周围神经系统(PNS)有直接的影响。PNS中的Batrachotoxin会增加静息细胞膜对钠离子的通透性(选择性和不可逆),而不会改变钾或钙的浓度。这种钠的流入使之前极化的细胞膜去极化。Batrachotoxin还通过增加通道对较大阳离子的通透性来改变离子通道的离子选择性。电压敏感的钠离子通道在静止膜电位下仍持续活跃。Batrachotoxin通过永久阻断神经信号传输到肌肉来致死。
Batrachotoxin与神经细胞的钠离子通道结合,且不可逆地打开钠离子通道,并使其无法关闭,导致神经元不能再发送讯号而使之瘫痪。
虽然Batrachotoxin通常被归类为神经毒素,但其对心肌有显著的影响。这些作用类似于地高辛的心脏毒性作用,地高辛是一种在毛地黄植物中发现的毒药。Batrachotoxin会干扰心脏传导,引起心律不整、期外收缩、心室颤动和其他导致心脏骤停的变化。Batrachotoxin会诱导神经和肌肉中乙酰胆碱的大量释放以及对突触小泡的破坏。Batrachotoxin R比与其相关的Batrachotoxin A毒性更大。
神经和肌肉的结构变化是由于钠离子的大量流入导致通透性改变。有人提出可能对中枢神经系统(CNS)也有影响,尽管目前尚不清楚这种影响可能是什么。
Batrachotoxin的活性与温度有关,在37°C(99°F)时活性最大。它的活性在碱性pH值下也更大,这表明未质子化的形式可能更具活性。
治疗
[编辑]目前,尚无治疗箭毒蛙碱毒素中毒的有效解毒剂。[8]藜芦碱、乌头碱和梫木毒素(如箭毒蛙碱)是脂溶性毒物,它们同样会改变钠离子通道的离子选择性,表明它们是作用在共同的部位。由于这些相似性,箭毒蛙碱中毒的治疗最好可以仿照以上其中一种毒药的治疗方式。例如可以仿照洋地黄中毒的治疗方式,因为它也会产生一些类似的心脏毒性作用。
虽然它不是解毒剂,但可以通过河豚毒素[8](一种非竞争性抑制剂)或石房蛤毒素[来源请求]来防止或逆转膜的去极化。某些麻醉剂可以作为这种生物碱毒物的受体拮抗剂,而其他局部麻醉剂可通过作为竞争性拮抗剂完全阻断其作用。
参见
[编辑]参考来源
[编辑]- ^ Daly, J. W.; Journal of the American Chemical Society 1965, V87(1), P124-6 CAPLUS
- ^ The Merck Index. Entry 1009. p. 167.
- ^ Märki, F.; Witkop, B. The venom of the Colombian arrow poison frogPhyllobates bicolor. Experientia. 1963, 19 (7): 329–338. PMID 14067757. S2CID 19663576. doi:10.1007/BF02152303 (英语).
- ^ 4.0 4.1 Tokuyama, T.; Daly, J.; Witkop, B. Structure of Batrachotoxin, a steroidal alkaloid from the Colombian arrow poison frog, Phyllobates aurotaenia, and partial synthesis of Batrachotoxin and its analogs and homologs. J. Am. Chem. Soc. 1969, 91 (14): 3931–3933. PMID 5814950. doi:10.1021/ja01042a042.
- ^ 5.0 5.1 Tokuyama, T.; Daly, J.; Witkop, B.; Karle, I. L.; Karle, J. The structure of Batrachotoxinin A, a novel steroidal alkaloid from the Columbian arrow poison frog, Phyllobates aurotaenia. J. Am. Chem. Soc. 1968, 90 (7): 1917–1918. PMID 5689118. doi:10.1021/ja01009a052.
- ^ Wang, S. Y.; Mitchell, J.; Tikhonov, D. B.; Zhorov, B. S.; Wang, G. K. How Batrachotoxin modifies the sodium channel permeation pathway: Computer modeling and site-directed mutagenesis. Mol. Pharmacol. 2006, 69 (3): 788–795. PMID 16354762. S2CID 6343011. doi:10.1124/mol.105.018200.
- ^ Wang, S. Y.; Tikhonov, Denis B.; Mitchell, Jane; Zhorov, Boris S.; Wang, Ging Kuo. Irreversible Block of Cardiac Mutant Na+ Channels by Batrachotoxin Channels. Channels. 2007, 1 (3): 179–188. PMID 18690024. doi:10.4161/chan.4437
 .
.
- ^ 8.0 8.1 Poison Dart Frog - an overview | ScienceDirect Topics. www.sciencedirect.com. [2022-11-14]. (原始内容存档于2022-11-14).
