精子发生
此条目需要补充更多来源。 (2024年6月14日) |

精子发生(英语:spermatogenesis)是指有性生殖的雄性动物的生殖细胞在睾丸中的生精小管中发育为单倍体精子的过程。这一过程始于附着在生精小管基底膜的生殖细胞的有丝分裂[1]。这些生殖细胞被称为精原细胞。精原细胞分为增加生殖细胞数量的A型精原细胞和将要分化为初级精母细胞的B型精原细胞。人类的精原细胞(A0)经历七次有丝分裂(A1-A4、中间型、B型)分化为初级精母细胞。初级精母细胞减数分裂(第一次减数分裂)为两个次级精母细胞,次级精原细胞分别减数分裂(第二次减数分裂)为两个相同的单倍体精子细胞(spermatid),之后进一步成熟为精子[2]。精子细胞分化、变态、成熟的过程称为精子形成(spermiogenesis)。一个B型精原细胞通过上述过程产生四个单倍体的精子[3]。
精子发生是有性生殖的重要环节,适当的环境条件是精子发生正常进行的关键。DNA甲基化和组蛋白修饰在精子生成过程中发挥调控作用[4]。精子发生开始于青春期,之后一般终身持续进行,但随着年龄增长,产生的精子数量可能会有小幅降低(参见男性不育)。
精子发生起始于生精小管基底膜,细胞分裂、分化、成熟的同时沿生精小管移动并逐渐向内部迁移,最终向管腔释放成熟的精子。精子发生过程中的分裂具有同步性,使生精小管的横断面呈现出不同发育阶段对应的特定时相。生精小管上不同发育阶段的细胞形成的一段横切面的连续时相变化被称为生精上皮周期[5]。
意义
[编辑]精子发生过程产生成熟的雄性配子,即精子。在有性生殖过程中,精子与雌性配子(卵细胞)结合使其受精。受精过程中,两个单倍体的配子分别提供正常个体一半数量的染色体,重新组合成二倍体的受精卵。染色体数目改变通常会造成严重的胚胎发育障碍,为了保持后代染色体数量的稳定,配子的染色体数量必须减半。精子发生中的染色体数目异常可以引起人类的胚胎自然流产、先天性发育缺陷和认知障碍疾病(如唐氏综合征、克氏综合征)。

场所
[编辑]精子发生的起始阶段发生在睾丸中,之后逐渐转移至附睾,发育中的配子细胞在附睾中成熟,并储存直到射精排出。睾丸中的生精小管是精子发生的起点,生精小管内壁上的精原细胞朝着中心分裂——从内壁逐渐迁移至管腔——来产生未成熟的精子[2],之后依次流入直精小管、睾丸网,最终通过15—20个输出小管进入附睾中成熟。精子生成通常需要在低于体温1—8°C的较低温度下才能产生具有活性的精子,因此精子发生的场所(睾丸/阴囊)所处的温度调节十分重要[6]。不过,临床上发现小幅的温度波动(如使用运动护裆带来的温度变化)对精子的活力和数量没有负面影响。
值得注意的是,精子发生并不能产生具有授孕能力的精子。精子最后的成熟阶段,即获能,发生在雌性的子宫或输卵管内。在最后的获能阶段,精子失去顶体表面的糖蛋白和精液蛋白,使其得以发生顶体反应从而与卵子融合。[7]
周期
[编辑]根据不同的测定方法,人类精子发生周期的时间估算从74天(以氚标记活检测定)[8]到120天(以表观遗传时钟测定)[9]不等。精原细胞有丝分裂增殖大约需要16天;第一次减数分裂约需要24天,第二次减数分裂则仅需要数个小时;精细胞变态形成精子还需要约24天。如果计入精子在生精小管中转运所需的时间,精子的形成大约需要三个月。男性的(一对)睾丸每天能产生2—3亿个精细胞[10],但其中只有约一半(即1亿)可以形成具有活力的精子[11]。
阶段
[编辑]人类精子发生的过程可以根据细胞类型划分为数个阶段。下表中除初级精母细胞中“倍性/DNA拷贝数/染色体数量”是DNA复制后、细胞分裂前的计数外,其他细胞的计数是指在DNA复制和细胞分裂之前的计数(即G1期)。
| 细胞类型 | 倍性/染色体数量(人类) | DNA拷贝数/染色单体数量(人类) | 进入下一阶段所经历的过程 |
|---|---|---|---|
| 精原细胞(Ad型、Ap型和B型) | 二倍体(2N)/46 | 2C/46 | 精母细胞发生(有丝分裂) |
| 初级精母细胞 | 二倍体(2N)/46 | 4C/46 | 精细胞发生(第一次减数分裂) |
| 2个次级精母细胞 | 单倍体(N)/23 | 2C/46 | 精细胞发生(第二次减数分裂) |
| 4个精细胞 | 单倍体(N)/23 | 1C/23 | 精子形成 |
| 4个精子 | 单倍体(N)/23 | 1C/23 | 精子释放 |
精母细胞发生
[编辑]
雄性配子发生的过程被称为精母细胞发生。在这一过程中,位于生精小管的基底室(basal compartment)的精原细胞发生有丝分裂,形成两个二倍体的中间体,称为初级精母细胞。根据精原细胞的核形态的不同可以将其分为A型精原细胞和B型精原细胞。[12]A型精原细胞的异染色质较少,分化程度较低;B型精原细胞异染色质比例较高,说明其转录活动较低,分化程度较高。A型精原细胞可以根据其细胞形态进一步分为Ad(dark)精原细胞和Ap(pale)精原细胞:Ad细胞位于生精小管基底膜上,分裂活动较低,一般认为是干细胞和储备精原细胞,是其他Ad精原细胞和Ap精原细胞的祖细胞;Ap精原细胞不断分裂并逐渐向生精小管的管腔方向迁移,最终产生B型精原细胞。B型精原细胞是形成精母细胞的祖细胞。在人类中,A型精原细胞(A0)一般经过六轮分裂(A1-A4、中间型)形成B型精原细胞。
初级精母细胞迁移至生精小管的近腔室(adluminal compartment)进行DNA复制,然后发生第一次减数分裂,产生两个单倍体的次级精母细胞,接着发生第二次减数分裂产生单倍体的精细胞。第一次减数分裂的前期长达22—24天,因此成为组织切片中比例最多的细胞。根据初级精母细胞的细胞核的染色特征,可以将前期分为五个阶段:
- 细线期(凝集期):此时DNA已开始复制,染色质初步螺旋化形成线状,为偶线期做准备。
- 偶线期(合线期):染色质进一步螺旋化,偶线期DNA完成复制,同源染色体发生联会。
- 粗线期(重组期):同源染色体紧贴合并(假减数),发生同源染色体重组,可以看到清晰的核仁
- 双线期:同源染色体分离形成四分体,不完全分开的部分称为交叉,染色体上大量的转录泡形成典型的灯刷染色体结构
- 缩线期(终变期):同源染色体最终完全脱离,核膜、核仁消失,准备形成纺锤体进行减数分裂
精母细胞发生的过程通过染色体联会和同源染色体重组增加配子的遗传多样性。DNA损伤应答(DDR)是精母细胞发生中的重要机制。DNA损伤修复的关键蛋白FMRP在精母细胞发生的减数分裂过程中结合在染色体上调控DNA损伤应答[13]。
精母细胞发生中细胞进行不完全分裂,子代细胞通过细胞质间桥相连,使细胞发育的状态同步化。精原细胞不断通过有丝分裂补充自身的数量,为精母细胞发生提供持续的精原细胞供应,确保不断进行的精母细胞发生不会耗尽睾丸中的精原细胞[14]。
精细胞发生
[编辑]精细胞生成是次级精母细胞产生精细胞的过程。精母细胞发生中产生的次级精母细胞迅速进入第二次减数分裂产生单倍体的圆形精细胞。这一阶段十分短暂,因此在组织切片中很难观察到次级精母细胞。
精子形成
[编辑]在精子形成阶段中,精细胞的一个中心粒上的微管延伸形成尾部,延伸出的微管形成轴丝,相应的中心粒形成毛基体,从而使中心体减半[15]。精细胞延伸的同时,DNA首先与特定的碱性核蛋白结合,之后逐步替换为与精蛋白紧密结合,包装为高度浓缩、失去转录活性的染色质。包裹浓缩细胞核的高尔基体在中心粒迁移方向相反的一极积累顶体颗粒。这一阶段被称为高尔基期。
随着囊泡和顶体颗粒的扩张,顶体颗粒融合形成包裹细胞核前半部分的顶体。线粒体围绕轴丝的前端(中段)排列使其变粗,为精子尾部摆动供能。同时,精子的细胞核逐渐伸长,朝向发生定向的改变(头部朝向生精小管的管壁,尾部朝管腔延伸)。这一阶段被称为顶体期。
最终在睾酮的诱导下,精细胞进一步成熟,除去残余的胞浆和细胞器。排出的胞浆称为残余体,将由周围的支持细胞通过胞吞作用吸收。这一阶段称为成熟期。此阶段的成熟精细胞还不具有运动能力。成熟的精细胞从支持细胞上释放到生精小管的管腔中的过程称为精子释放。精细胞变形为精子的过程需要12—24天。
在生精小管的蠕动帮助下,不具运动能力的成熟精细胞随支持细胞分泌的睾丸液转运至附睾中。成熟精细胞在附睾中成为具有游动能力的精子。但精子并不依靠自身的游动通过男性生殖系统的剩余部分,而是借由肌肉收缩被排出体外。
支持细胞的作用
[编辑]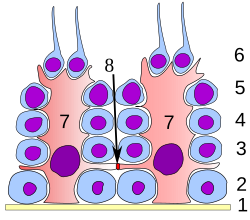
尚未经历精子形成的精细胞附着于塞尔托利氏细胞位于管腔一侧的顶部。
图中序号:1.基底膜,2.精原细胞,3.初级精母细胞,4.次级精母细胞,5.精细胞,6.成熟精细胞(精子),7.支持细胞(塞尔托利氏细胞),8 血睾屏障
塞尔托利氏细胞又称支持细胞。支持细胞为精子发生过程提供结构性和营养的支持作用。在精子发生的各个阶段,生精细胞都与支持细胞保持紧密接触。每一个支持细胞的都从生精小管的基底膜延伸至管腔,但这一结构在光镜下通常难以分辨。
支持细胞在精子发生过程中发挥多种功能,它们以下列方式支持配子的发育:
- 形成血睾屏障,从而维持精子发育和成熟所需的环境
- 分泌减数分裂诱发物(meiosis-inducing substance,MIS)
- 分泌睾丸液
- 分泌以抑制素(inhibin)等肽类激素为代表的激素,参与下丘脑-垂体-性腺轴对精子发生的调控
- 通过胞吞作用清理精子形成中的胞浆残余体
- 分泌抗米勒管激素(Anti-Müllerian hormone,AMH)使副中肾管退化,引起胚胎性别分化[16]
- 通过血睾屏障形成精子发育所需的免疫豁免环境
- 参与调节精原细胞的更新和维持
支持细胞在青春期后不再进行细胞分裂,从而与相邻的生殖细胞保持稳定的位置关系[17]。虽然支持细胞无法增殖,但其抗逆能力(如X射线、营养不良和感染)非常高,因此不易因环境因素受损[18]。
细胞间黏附因子ICAM-1和可溶性ICAM-1对形成血睾屏障的紧密连接具有抑制作用[19]。ICAM-2与精细胞在支持细胞顶部(朝向管腔一侧)的附着有关[19]。
影响因素
[编辑]精子发生对环境的波动极为敏感,尤其是激素和温度的变化。睾酮主要由生精小管外围的睾丸间质细胞分泌,生精小管中的性激素结合蛋白可以富集睾酮,使局部的睾酮浓度满足维持精子发生的需要。
人类和一些动物的生精上皮对温度升高较为敏感,即便是正常体温也会对精子发生造成不良影响。此外,大多数哺乳动物精母细胞中的DNA聚合酶β和重组酶需要特殊的最适温度,使得精子无法在核心体温下成熟[20]。因此哺乳动物的睾丸通常位于体外的囊状皮肤结构中,即阴囊。提睾肌和阴囊肉膜通过调控阴囊的血流量[21]和位置,保持睾丸处于精子发生的最适温度下。人类精子发生的最适温度相较于体温要低2°C,小鼠则要低8°C。
睾丸的动脉血和静脉血的热交换是维持睾丸温度稳定的重要机制之一。睾丸静脉在两个区域盘绕精索内动脉,这种特殊的解剖结构增加了流入睾丸的动脉血与回流的静脉血之间的接触时间和热交换程度,一定程度上解释了犬和羊中观察到的主动脉和睾丸动脉血之间的温度差异。此外,精索内动脉的前1/3段呈现脉压差的降低[22][23]。此外,精母细胞中重组酶水平的降低可能是睾丸退行性改变的重要因素[24]。
营养不良(如缺乏维生素E)、合成类固醇、重金属(如镉和铅)、X射线、二𫫇英、酒精以及感染性疾病都可能对精子发生的速率产生不利影响[25]。此外,氧化应激易对生殖细胞造成DNA损伤,这些损伤可能显著影响男性的生育力[26]。也有报道发现杀虫剂的暴露水平会影响精子发生[27]。
激素调控
[编辑]精子发生的激素控制随物种而不同。人类精子发生的激素控制机制尚未完全揭示,但已知男性青春期的下丘脑-垂体-性腺轴的活动启动了精子发生。垂体受损时,促卵泡激素(FSH)和睾酮也可以直接启动精子生成[28]。黄体生成素(LH)可以促进生殖腺的睾酮分泌,但对精子生成似乎没有直接的作用[28][29]。
FSH刺激支持细胞形成血睾屏障和产生性激素结合蛋白(ABP)。性激素结合蛋白是维持生精过程需要的局部高睾酮水平的关键。睾丸中的睾酮水平约为外周血中的20—100或50—200倍,不过健康男性之间的睾酮水平可能存在5到10倍的差距[30][31]。睾酮水平呈现节律性的周期变化,一般在晨起时达到峰值,这也解释了男性的晨勃现象。青年男性的睾酮水平更高。FSH可能启动了睾丸的睾酮生成和精子发生,但在启动后只需要睾酮即可维持精子发生的进行[28]。不过FSH水平的升高可以通过减少A型精原细胞的凋亡来增加精细胞的生成数量。抑制素(inhibin)通过降低FSH的水平来发挥功能。啮齿类动物中的研究发现促性腺激素(FSH和LH)可以通过抑制精母细胞的促凋亡信号转导来促进精子发生[32]。
支持细胞本身也通过分泌激素参与精子生成的调控。支持细胞可以产生雌二醇和抑制素。睾丸间质细胞除了产生睾酮外,也可以产生相对较少的雌二醇。在动物模型中发现雌激素对于精子发生而言是必要的[33][34],然而雌激素不敏感综合征(α雌激素受体缺陷)的男性患者表现为正常的精子计数,但精子成活率较低,患者的生育力不明[35]。过高的雌激素水平可能导致睾丸中过量睾酮分泌和促性腺激素分泌的抑制[36],从而损害精子发生。催乳素与精子发生也有一定的相关性,正常范围的催乳素水平可以侧面反映有效精子生成的进行[29][37]。
与卵细胞发生的对比
[编辑]与女性产生卵细胞的过程相比,精原细胞形成具有游动能力的精子的过程中失去了绝大部分的细胞质和其中包含的细胞器,这些组分均在卵细胞中得以保留。一个初级精母细胞会产生四个精子,而对应的初级卵母细胞最终仅产生一个卵细胞。在人类中,女性的卵原细胞在胎儿卵巢中即转化为初级卵母细胞,在青春期前停留在第一次减数分裂的晚期(双线期),出生后卵母细胞的数量不断减少;而男性的精原细胞则要到青春期才启动精母细胞的生成,精子发生中的减数分裂和分化持续进行,并且可以维持终身。精子发生过程中由于性染色体无法配对,因此不会发生性染色体的重组和转录。男性的精子发生也不具有女性卵细胞发生的激素调节周期那样明显的周期性。
生精障碍
[编辑]精子发生的障碍可能导致少精症,即精液中的精子浓度偏低。少精症是男性不育的常见表现之一。
可能导致生精障碍的常见原因之一是隐睾,即睾丸不完全下降至阴囊中的情况。通常在胎儿时期睾丸即下降到阴囊中,如果在出生后三个月以上睾丸仍未降至阴囊中,则睾丸所处的温度(37°C)可能会阻碍精子的正常产生。这一类男性不育症可以通过外科手术治疗改善。
其他影响精子发生的因素包括电离辐射、药物、酗酒、重金属、精神压力和营养不良。此外,纤毛相关的疾病(如原发性纤毛运动不良症)除了影响呼吸系统外还会影响正常精子的形成,主要表现为精子缺乏活动能力。
参考文献
[编辑]- ^ de Kretser, D. M.; Loveland, K. L.; Meinhardt, A.; Simorangkir, D.; Wreford, N. Spermatogenesis. Human Reproduction (Oxford, England). 1998-04,. 13 Suppl 1 [2024-06-11]. ISSN 0268-1161. PMID 9663765. doi:10.1093/humrep/13.suppl_1.1. (原始内容存档于2024-06-11).
- ^ 2.0 2.1 Sharma, Sachin; Hanukoglu, Aaron; Hanukoglu, Israel. Localization of epithelial sodium channel (ENaC) and CFTR in the germinal epithelium of the testis, Sertoli cells, and spermatozoa. Journal of Molecular Histology. 2018-04, 49 (2) [2024-06-11]. ISSN 1567-2387. PMID 29453757. doi:10.1007/s10735-018-9759-2. (原始内容存档于2024-06-11).
- ^ The Spermatozoön. Human Anatomy. [2024-06-10]. (原始内容存档于2018-07-01) (英语).
- ^ Song, Ning; Liu, Jie; An, Shucai; Nishino, Tomoya; Hishikawa, Yoshitaka; Koji, Takehiko. Immunohistochemical Analysis of Histone H3 Modifications in Germ Cells during Mouse Spermatogenesis. Acta Histochemica Et Cytochemica. 2011-08-27, 44 (4) [2024-06-11]. ISSN 1347-5800. PMC 3168764
 . PMID 21927517. doi:10.1267/ahc.11027. (原始内容存档于2024-09-20).
. PMID 21927517. doi:10.1267/ahc.11027. (原始内容存档于2024-09-20).
- ^ Schulze, W. Evidence of a wave of spermatogenesis in human testis. Andrologia. 1982, 14 (2) [2024-06-11]. ISSN 0303-4569. PMID 7103139. doi:10.1111/j.1439-0272.1982.tb03124.x. (原始内容存档于2024-06-11).
- ^ Scrotum. Britannica. 2024-06-01 [2024-06-10]. (原始内容存档于2015-04-29) (英语).
- ^ Johnson, M. H.; Everitt, Barry J. Essential reproduction 6th ed. Malden, Mass: Blackwell Pub. 2007. ISBN 978-1-4051-1866-8. OCLC 76074156.
- ^ Heller, C. H.; Clermont, Y. KINETICS OF THE GERMINAL EPITHELIUM IN MAN. Recent Progress in Hormone Research. 1964, 20 [2024-06-11]. ISSN 0079-9963. PMID 14285045. (原始内容存档于2024-06-11).
- ^ Forster, Peter; Hohoff, Carsten; Dunkelmann, Bettina; Schürenkamp, Marianne; Pfeiffer, Heidi; Neuhuber, Franz; Brinkmann, Bernd. Elevated germline mutation rate in teenage fathers. Proceedings. Biological Sciences. 2015-03-22, 282 (1803) [2024-06-11]. ISSN 1471-2954. PMC 4345458
 . PMID 25694621. doi:10.1098/rspb.2014.2898. (原始内容存档于2019-10-25).
. PMID 25694621. doi:10.1098/rspb.2014.2898. (原始内容存档于2019-10-25).
- ^ Padubidri, VG; Daftary, SN (编). Shaw's Textbook of Gynaecology 15th. Elsevier (A Divisionof Reed Elsevier India Pvt. Limited). 2011: 201. ISBN 978-81-312-2548-6.
- ^ Johnson, L.; Petty, C. S.; Neaves, W. B. Further quantification of human spermatogenesis: germ cell loss during postprophase of meiosis and its relationship to daily sperm production. Biology of Reproduction. 1983-08, 29 (1) [2024-06-11]. ISSN 0006-3363. PMID 6615966. doi:10.1095/biolreprod29.1.207. (原始内容存档于2024-06-11).
- ^ de Kretser, David M.; Loveland, Kate; O’Bryan, Moira. Spermatogenesis. Endocrinology: Adult and Pediatric. Elsevier. 2016: 2325–2353.e9 [2024-06-14]. ISBN 978-0-323-18907-1. doi:10.1016/b978-0-323-18907-1.00136-0. (原始内容存档于2024-07-05) (英语).
- ^ Alpatov, Roman; Lesch, Bluma J.; Nakamoto-Kinoshita, Mika; Blanco, Andres; Chen, Shuzhen; Stützer, Alexandra; Armache, Karim J.; Simon, Matthew D.; Xu, Chao; Ali, Muzaffar; Murn, Jernej. A chromatin-dependent role of the fragile X mental retardation protein FMRP in the DNA damage response. Cell. 2014-05-08, 157 (4) [2024-06-11]. ISSN 1097-4172. PMC 4038154
 . PMID 24813610. doi:10.1016/j.cell.2014.03.040. (原始内容存档于2024-10-09).
. PMID 24813610. doi:10.1016/j.cell.2014.03.040. (原始内容存档于2024-10-09).
- ^ Fishelson, Lev; Gon, Ofer; Holdengreber, Vered; Delarea, Yakob. Comparative spermatogenesis, spermatocytogenesis, and spermatozeugmata formation in males of viviparous species of clinid fishes (Teleostei: Clinidae, Blennioidei). Anatomical Record (Hoboken, N.J.: 2007). 2007-03, 290 (3) [2024-06-11]. ISSN 1932-8486. PMID 17525946. doi:10.1002/ar.20412. (原始内容存档于2024-07-28).
- ^ Avidor-Reiss, Tomer; Khire, Atul; Fishman, Emily L.; Jo, Kyoung H. Atypical centrioles during sexual reproduction. Frontiers in Cell and Developmental Biology. 2015-04-01, 3. ISSN 2296-634X. doi:10.3389/fcell.2015.00021 (English).
- ^ Hadley, Mac E.; Levine, Jon E. Endocrinology 6th. Upper Saddle River, NJ: Prentice Hall. 2007: 369. ISBN 978-0-13-187606-4.
- ^ Anastasi; et al. Trattato di anatomia umana, volume II. Edi.Ermes. 2007. ISBN 978-88-7051-286-1.
- ^ Luis C. Junqueira; José Carneiro. Compendio di istologia 5. Piccin. 2006. ISBN 88-299-1817-2.
- ^ 19.0 19.1 Xiao, Xiang; Mruk, Dolores D.; Cheng, C. Yan. Intercellular adhesion molecules (ICAMs) and spermatogenesis. Human Reproduction Update. 2013, 19 (2) [2024-06-11]. ISSN 1460-2369. PMC 3576004
 . PMID 23287428. doi:10.1093/humupd/dms049. (原始内容存档于2024-04-11).
. PMID 23287428. doi:10.1093/humupd/dms049. (原始内容存档于2024-04-11).
- ^ SPERMATOGENESIS. University of Wyoming. [2024-06-11]. (原始内容存档于2024-07-15) (英语).
- ^ Harrison, R. G.; Weiner, J. S. Vascular patterns of the mammalian testis and their functional significance. The Journal of Experimental Biology. 1949-10, 26 (3) [2024-06-12]. ISSN 0022-0949. PMID 15407652. doi:10.1242/jeb.26.3.304. (原始内容存档于2024-10-08).
- ^ Kandeel, F. R.; Swerdloff, R. S. Role of temperature in regulation of spermatogenesis and the use of heating as a method for contraception. Fertility and Sterility. 1988-01, 49 (1) [2024-06-12]. ISSN 0015-0282. PMID 3275550. doi:10.1016/s0015-0282(16)59640-x. (原始内容存档于2024-01-07).
- ^ Cameron, R. D.; Blackshaw, A. W. The effect of elevated ambient temperature on spermatogenesis in the boar. Journal of Reproduction and Fertility. 1980-05, 59 (1) [2024-06-14]. ISSN 0022-4251. PMID 7401033. doi:10.1530/jrf.0.0590173. (原始内容存档于2024-06-14).
- ^ Hotta, Y.; Fujisawa, M.; Tabata, S.; Stern, H.; Yoshida, S. The effect of temperature on recombination activity in testes of rodents. Experimental Cell Research. 1988-09, 178 (1) [2024-06-12]. ISSN 0014-4827. PMID 2900772. doi:10.1016/0014-4827(88)90387-4. (原始内容存档于2024-06-12).
- ^ Jenardhanan, Pranitha; Panneerselvam, Manivel; Mathur, Premendu P. Effect of environmental contaminants on spermatogenesis. Seminars in Cell & Developmental Biology. 2016-11, 59 [2024-06-12]. ISSN 1096-3634. PMID 27060550. doi:10.1016/j.semcdb.2016.03.024. (原始内容存档于2024-06-15).
- ^ Lewis, S. E. M.; Aitken, R. J. DNA damage to spermatozoa has impacts on fertilization and pregnancy. Cell and Tissue Research. 2005-10-18, 322 (1). ISSN 0302-766X. doi:10.1007/s00441-005-1097-5 (英语).
- ^ Mehrpour, Omid; Karrari, Parissa; Zamani, Nasim; Tsatsakis, Aristides M.; Abdollahi, Mohammad. Occupational exposure to pesticides and consequences on male semen and fertility: A review. Toxicology Letters. 2014-10, 230 (2). doi:10.1016/j.toxlet.2014.01.029 (英语).
- ^ 28.0 28.1 28.2 William J. Kraemer; A. D. Rogol. The Encyclopaedia of Sports Medicine: An IOC Medical Commission Publication, The Endocrine System in Sports and Exercise. John Wiley & Sons. 15 April 2008: 286–. ISBN 978-0-470-75780-2.
- ^ 29.0 29.1 Fody, E. P.; Walker, E. M. Effects of drugs on the male and female reproductive systems. Annals of Clinical and Laboratory Science. 1985, 15 (6) [2024-06-12]. ISSN 0091-7370. PMID 4062226. (原始内容存档于2024-10-08).
- ^ Wolf-Bernhard Schill; Frank H. Comhaire; Timothy B. Hargreave. Andrology for the Clinician. Springer Science & Business Media. 26 August 2006: 76–. ISBN 978-3-540-33713-3.
- ^ Eberhard Nieschlag; Hermann M. Behre; Susan Nieschlag. Testosterone: Action, Deficiency, Substitution. Cambridge University Press. 26 July 2012: 130–. ISBN 978-1-107-01290-5..
- ^ Pareek, Tej K.; Joshi, Ayesha R.; Sanyal, Amartya; Dighe, Rajan R. Insights into male germ cell apoptosis due to depletion of gonadotropins caused by GnRH antagonists. Apoptosis: An International Journal on Programmed Cell Death. 2007-06, 12 (6) [2024-06-12]. ISSN 1360-8185. PMID 17268770. doi:10.1007/s10495-006-0039-3. (原始内容存档于2024-06-12).
- ^ O'Donnell, L.; Robertson, K. M.; Jones, M. E.; Simpson, E. R. Estrogen and spermatogenesis. Endocrine Reviews. 2001-06, 22 (3) [2024-06-12]. ISSN 0163-769X. PMID 11399746. doi:10.1210/edrv.22.3.0431. (原始内容存档于2024-06-12).
- ^ Carreau, Serge; Bouraima-Lelong, Helene; Delalande, Christelle. Role of estrogens in spermatogenesis. Frontiers in Bioscience (Elite Edition). 2012-01-01, 4 (1) [2024-06-12]. ISSN 1945-0508. PMID 22201851. doi:10.2741/e356. (原始内容存档于2024-06-12).
- ^ Smith, E. P.; Boyd, J.; Frank, G. R.; Takahashi, H.; Cohen, R. M.; Specker, B.; Williams, T. C.; Lubahn, D. B.; Korach, K. S. Estrogen resistance caused by a mutation in the estrogen-receptor gene in a man. The New England Journal of Medicine. 1994-10-20, 331 (16) [2024-06-12]. ISSN 0028-4793. PMID 8090165. doi:10.1056/NEJM199410203311604. (原始内容存档于2024-06-12).
- ^ Edmund S. Sabanegh Jr. Male Infertility: Problems and Solutions. Springer Science & Business Media. 20 October 2010: 83–. ISBN 978-1-60761-193-6.
- ^ Spaggiari, Giorgia; Costantino, Francesco; Granata, Antonio R. M.; Tagliavini, Simonetta; Canu, Giulia; Varani, Manuela; De Santis, Maria Cristina; Roli, Laura; Trenti, Tommaso; Simoni, Manuela; Santi, Daniele. Prolactin and spermatogenesis: new lights on the interplay between prolactin and sperm parameters. Endocrine. 2023-08, 81 (2). ISSN 1559-0100. PMID 37140814. doi:10.1007/s12020-023-03375-x.
延伸阅读
[编辑]- Okano, Tsukasa; Ishiniwa, Hiroko; Onuma, Manabu; Shindo, Junji; Yokohata, Yasushi; Tamaoki, Masanori. Effects of environmental radiation on testes and spermatogenesis in wild large Japanese field mice ( Apodemus speciosus ) from Fukushima. Scientific Reports. 23 March 2016, 6 (1): 23601. Bibcode:2016NatSR...623601O. PMC 4804236
 . PMID 27005329. doi:10.1038/srep23601.
. PMID 27005329. doi:10.1038/srep23601. - Johnson, L.; Blanchard, T.L.; Varner, D.D.; Scrutchfield, W.L. Factors affecting spermatogenesis in the stallion. Theriogenology. November 1997, 48 (7): 1199–1216. PMID 16728209. doi:10.1016/s0093-691x(97)00353-1.
- Bardin, C.W. Pituitary-testicular axis. Yen, S.S.C.; Jaffee, R.B. (编). Reproductive Endocrinology 3rd. Philadelphia: WB Saunders. 1991. ISBN 0721632068.
- Chambers, Christopher V.; Shafer, Mary-Ann; Adger, Hoover; Ohm-Smith, Marilyn; Millstein, Susan G.; Irwin, Charles E.; Schachter, Julius; Sweet, Richard. Microflora of the urethra in adolescent boys: Relationships to sexual activity and nongonococcal urethritis. The Journal of Pediatrics. February 1987, 110 (2): 314–321. PMID 3100755. doi:10.1016/s0022-3476(87)80180-4.
- Czyba, J.C.; Girod, C. Development of normal testis. Hafez, E.S.E. (编). Descended and Cryptorchid Testis. The Hague: Martinus Nijhoff. 1980. ISBN 9024723337.
- Whitmore, Willet F.; Karsh, Lawrence; Gittes, Ruben F. The Role of Germinal Epithelium and Spermatogenesis in the Privileged Survival of Intratesticular Grafts. Journal of Urology. October 1985, 134 (4): 782–786. PMID 2863395. doi:10.1016/s0022-5347(17)47438-6.
外部链接
[编辑]- Spermatogenesis - male reproductive physiology (页面存档备份,存于互联网档案馆) - Am Fam Physician 2000;62:1095.
- Spermatogenesis animation (页面存档备份,存于互联网档案馆)
