孤电子对
外观
(重定向自孤偶電子對)

孤电子对(英语:lone pair,或称孤对电子)是不与其他原子结合或共享的以共价键成对价电子[1]。存在于原子的最外围电子壳层。可以使用路易斯结构来标识它们。
孤对电子在分子中的存在和分配影响分子的形状等,对氢原子组成的分子影响尤为显著。指分子中未成键的价电子对。
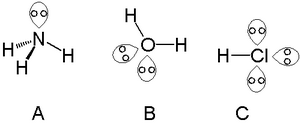
在氮族元素原子中可以找到一个孤电子对,例如氨中的氮,在氧族元素原子中可以找到两个孤电子对,例如在水中的氧,而卤素可以携带三个孤电子对,例如在氯化氢中。
在价层电子对互斥理论(VSEPR理论)中,水中氧原子上的电子对形成四面体的顶点,而孤电子对在四个顶点中的两个上。 H–O–H键角为104.5°,小于四面体角的109°预测值,这可以通过孤电子对之间的排斥相互作用来解释[2][3][4]。
参见
[编辑]参考文献
[编辑]| 这是一篇与化学相关的小作品。您可以通过编辑或修订扩充其内容。 |
