消化作用
此条目需要精通或熟悉相关主题的编者参与及协助编辑。 (2016年5月7日) |
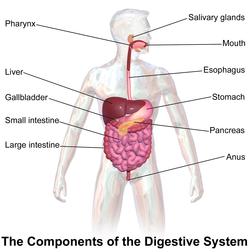
| 消化系统 | |
|---|---|
 | |
| 标识字符 | |
| 拉丁文 | systema digestorium |
| MeSH | D004063 |
| 《解剖学术语》 [在维基数据上编辑] | |
消化作用(digestion)简称消化,是指异营生物将食物(大分子)分解成足够小的水溶性分子(小分子),可以溶解在血浆,让身体能够吸收利用的过程。有些动物会透过小肠吸收小分子,带到血液系统中。
消化作用是生物异化作用(分解代谢)的一环,可以分为两个阶段:首先借由机械性的作用(机械消化,mechanical digestion)或称物理消化,将食物碎裂成小裂片;其次是化学性的作用(化学消化,chemical digestion),经由酶的催化,将大分子水解成小分子单体。无法消化的残渣则会再排出体外。
大多数食物中所含的有机物包括蛋白质、脂肪和碳水化合物。由于这些大分子聚合物无法穿过细胞膜进入细胞内,而且动物需要用单体来合成自身身体所需的聚合物,因此动物需要借由消化作用将食物中的大分子分解成单体。例如将蛋白质分解为氨基酸,多糖及双糖分解为单糖,脂肪分解为甘油及脂肪酸等。
消化系统
[编辑]最简单的生命体,例如原生动物,会利用扩散、主动运输或胞吞作用而将食物颗粒直接从周围环境中送入细胞内,再以酵素分解而获取营养物,这样的方式称为胞内消化。胞内消化不需要机械性裂解食物的过程,也不需要消化道或腔室,因此限制了此类动物的体型及复杂度,只能利用小的食物颗粒来获取营养素。
较大型的动物又演化出胞外消化的构造与机制。在消化道中,利用机械性及化学性的作用,可将大块食物分解成小分子的营养素,这些营养素被吸收后,参与代谢及合成作用。
原始的多细胞动物,例如水螅,其肠道是封闭的囊状物,只有一个开口作为入口及出口,称为消化循环腔,是一种不完全消化道(incomplete gut)。而自囊蠕虫类动物起,例如蠕虫、蛔虫,开始发育出肛门,具有口、咽、肛门及完整肠道,是完全消化道(complete gut)。完全消化道可使食物往单方向移动,不会与先前摄入的食物或废物混合,并且能循序渐进的处理食物,使食物在不同的步骤中被有效率的消化。
分泌系统
[编辑]
细菌利用几种不同的系统来获得外界其他有机体的养份。
通道传输系统
[编辑]在通道传输系统中,由几种蛋白质形成细菌细胞膜内部和外部之间的通道。通道传输系统包括三种蛋白质:ATP结合盒转运蛋白家族、膜融合蛋白(MFP)及外膜蛋白(OMP)。此分泌系统可以输送各种不同的分子:从离子、药物、到不同大小的蛋白质(20-900kDa)。所分泌的分子可以从大肠杆菌的肽大肠杆菌素(10 kDa)到萤光假单胞菌的细胞粘附蛋白(900 kDa)[1]。
分子注射器
[编辑]有些细菌(像沙门氏菌属、志贺氏菌属等)可以透过分子注射器(molecular syringe)注射养份或毒素到其他单细胞生物的细胞中。最早是在鼠疫杆菌中发现此机制,而且证实可以直接将毒素注射到宿主的细胞质内,而不只是分泌到细胞间质中[2]。
接合机制
[编辑]有些细菌有接合机制,可以交换DNA及蛋白质。此机制是在农杆菌中发现,利用此一机制引入Ti质粒到宿主的蛋白质中,因而引发冠缨[3]。
外膜囊泡释放
[编辑]除了利用上述的多蛋白质复合物外,革兰氏阴性菌还有另一种释放物质的方法:形成外膜囊泡[4]。
消化腔
[编辑]
消化腔的作用类似胃,一方面进行消化作用,另一方面也将营养分布到身体的各部分。细胞外消化就是发生在中央消化腔外,其内里是消化内皮层(gastrodermis),是上皮组织的内层,消化腔对外只有一个开口,具有摄取食物及排泄的功能,消化后的残余物及未消化物质从这个出口排到体外,这可以称为是不完全的肠道。
像捕蝇草之类可以用光合作用来产生食物的植物。其捕捉猎物并且消化的原因不像一般动物为了采集能量及碳元素,而是为了摄取必要的营养素(特别是氮和磷),这些营养素在其酸性沼泽栖息地是很不容易取得的[5]。

吞噬体
[编辑]吞噬体是因为吞噬作用吸收的物质,其周围形成的液泡。吞噬体是因为物质附近的细胞膜融合后所产生的。吞噬体也是细胞区室,致病微生物会在吞噬体内被杀死及消化。吞噬体在其成长过程会和溶酶体融合,最后形成吞噬溶酶体。人类体内的溶组织内阿米巴会吞噬红血球[6]。
脊椎动物消化作用的简介
[编辑]对大部分的脊椎动物而言,消化是在消化系统中多步骤的作用,从摄取食物(多半是其他的动植物)开始。消化作用也会包括一些物理程序及化学程序,可以分为以下四个步骤:
- 摄食:将食物放入口中(食物进入消化系统的起点)。
- 物理性及化学性的分解:口中咀嚼是物理性的分解,之后食团在胃肠中和水、胃酸、胆汁和酵素混合,将大型的分子分解为较简单的结构。
- 吸收:营养素从消化系统借由渗透、主动运输及扩散作用吸收到循环和淋巴毛细血管中。
- 排泄:最后无法消化的残余物质会透过排便离开消化道。
让消化作用正常作用的关键是消化系统中肌肉的动作,包括吞咽和蠕动运动。消化作用中的每一个步骤都需要能量。因此在从吸收的物质中取得能量之前,需要先消耗一些能量。消化作用需要能量的差异对于动物的生活方式、行为,甚至其外形都有很大的影响。像人类都和其他的人科动物有很大的不同(例如缺乏体毛、较小的颌骨和肌肉组织、齿列不同、肠子长度不同,是否会烹煮食物等)。
消化作用主要是发生在小肠中,大肠主要的作用是利用肠道菌种让无法消化的物质发酵,并且在排泄之前吸收残余物质中的水分。
哺乳类的消化作用
[编辑]哺乳类的消化准备工作是从头相开始,口腔会分泌唾液,胃部也会分泌消化酶。食物入口后,哺乳类会咀嚼食物,并且食物和唾液混合,此时开始了物理性及化学性的分解,之后食物进入胃部,继续其他的酵素作用。胃部也会继续进行物理性及化学性的分解,靠的是胃部的搅拌食物,以及让食物与胃酸和酵素混合。养份吸收是在胃部(胃酸)以及肠道(肠液、胰液、胆汁),最后残余物质会透过排便离开消化道(排遗作用)[7]。
不同物质的消化
[编辑]蛋白质的消化
[编辑]蛋白质是在胃进行消化,有三种主要的酵素:由胃部分泌的胃蛋白酶,以及胰脏分泌的胰蛋白酶及胰凝乳蛋白酶,可以将食物中的蛋白质分解为多肽,之后再由外肽酶及多肽酶分成氨基酸。不过胃和胰脏多半不会直接分泌消化酵素,而是分泌无活性的前体酶原。例如胰蛋白酶是以胰蛋白酶原的形式,由胰腺所分泌,再经由十二指肠的肠激酶活化成为胰蛋白酶。胰蛋白酶可以将蛋白质分解为较小的多肽。
脂质的消化
[编辑]有些脂质是从进入口腔起就开始消化,舌脂肪酶会将一些短链的脂质转换为甘油二酯。不过大部分的脂质是在小肠消化的[8]。小肠中脂肪的出现会产生激素,会让胰腺释放胰脂肪酶,让肝脏释放胆汁酸,有助于脂肪的乳化,可以以脂肪酸的形式吸收[8]。一莫耳脂肪(甘油三酯)在完全消化后会变成脂肪酸、甘油一酯、甘油二酯以及一些未分解甘油三酯的混合物,但其中不会有游离的甘油分子[8]。
糖类的消化
[编辑]人类可以消化的膳食淀粉是由葡萄糖单位组成的长链,称为直链淀粉,属于多糖。在消化时,唾液中和胰脏分泌的淀粉酶会破坏葡萄糖分子之间的链接,因此葡萄糖的长链会变短,产物会是结构较简单,可以被小肠吸收的葡萄糖及麦芽糖(二个葡萄糖组成的双糖)。
乳糖酶可以将乳糖分解为葡萄糖及半乳糖。小肠可以吸收葡萄糖及半乳糖。大约有65%的成年人分泌的乳糖酶不足,因此无法消化未发酵的乳制品,这称为乳糖不耐症。乳糖不耐症随着族群而不同,东亚血统人群超过90%有乳糖不耐症,而北欧后裔只有约5%有乳糖不耐症[9]。
蔗糖酶是分解蔗糖的酶,消化后会得到果糖及葡萄糖,可以由小肠持续的吸收。
DNA和RNA的消化
[编辑]DNA和RNA会由胰腺分泌的去氧核糖核酸酶(DNase)及核糖核酸酶(RNase)等核酸酶分解为核苷酸。
非破坏性消化
[编辑]有些营养素是复杂结构的分子(例如维生素B12),若分解其分子就会破坏营养素的功能。为了可以以非破坏性的方式消化维生素B12,唾液中的haptocorrin会和维生素B12形成强力的键结,当维生素B12进入胃部,haptocorrin可以保护B12不会被胃酸分解[10]。
维生素B12-haptocorrin复合物会从胃部通过幽门,进入十二指肠,胰腺蛋白酶会将haptocorrin和维生素B12分离,而维生素B12会和内在因子(IF)结合。维生素B12-内在因子复合物会再行进到小肠回肠段,而cubilin接受器会进行同化作用,使维生素B12-内在因子复合物进入血液系统[11]。
参见
[编辑]参考资料
[编辑]- ^ Wooldridge K (editor). Bacterial Secreted Proteins: Secretory Mechanisms and Role in Pathogenesis. Caister Academic Press. 2009. ISBN 978-1-904455-42-4.
- ^ Salyers, A. A. & Whitt, D. D. (2002). Bacterial Pathogenesis: A Molecular Approach, 2nd ed., Washington, D.C.: ASM Press. ISBN 978-1-55581-171-6
- ^ Cascales E & Christie P.J. The versatile Type IV secretion systems. Nat Rev Microbiol. 2003, 1 (2): 137–149. PMID 15035043. doi:10.1038/nrmicro753.
- ^ Chatterjee, SN and J Das. "Electron microscopic observations on the excretion of cell wall material by Vibrio cholerae." "J.Gen.Microbiol." "49" : 1-11 (1967) ; Kuehn, MJ and NC Kesty. "Bacterial outer membrane vesicles and the host-pathogen interaction." Genes Dev.and then the 19(22):2645-55 (2005)
- ^ Leege, Lissa. How does the Venus flytrap digest flies?. Scientific American. [2008-08-20].
- ^ Boettner, D. R.; Huston, C. D.; Linford, A. S.; Buss, S. N.; Houpt, E.; Sherman, N. E.; Petri, W. A. Entamoeba histolytica Phagocytosis of Human Erythrocytes Involves PATMK, a Member of the Transmembrane Kinase Family. PLoS Pathogens. 2008, 4 (1): e8. PMC 2211552
 . PMID 18208324. doi:10.1371/journal.ppat.0040008.
. PMID 18208324. doi:10.1371/journal.ppat.0040008.
- ^ Maton, Anthea; Jean Hopkins; Charles William McLaughlin; Susan Johnson; Maryanna Quon Warner; David LaHart; Jill D. Wright. Human Biology and Health. Englewood Cliffs, New Jersey, USA: Prentice Hall. 1993. ISBN 0-13-981176-1. OCLC 32308337.
- ^ 8.0 8.1 8.2 Digestion of fats (triacylglycerols). [2017-04-11]. (原始内容存档于2013-10-13).
- ^ Genetics Home Reference. US National Library of Medicine. US National Institutes of Health. [27 June 2015]. (原始内容存档于2016-01-25).
- ^ Nexo E, Hoffmann-Lücke E. Holotranscobalamin, a marker of vitamin B-12 status: analytical aspects and clinical utility. Am. J. Clin. Nutr. July 2011, 94 (1): 359S–365S. PMC 3127504
 . PMID 21593496. doi:10.3945/ajcn.111.013458.
. PMID 21593496. doi:10.3945/ajcn.111.013458.
- ^ Viola-Villegas N, Rabideau AE, Bartholomä M, Zubieta J, Doyle RP. Targeting the cubilin receptor through the vitamin B(12) uptake pathway: cytotoxicity and mechanistic insight through fluorescent Re(I) delivery. J. Med. Chem. August 2009, 52 (16): 5253–61. PMID 19627091. doi:10.1021/jm900777v.
